近日,我院李宇超副教授等在超分辨成像和纳米光操控研究中取得重要进展,他们将酵母细胞、造血干细胞或红细胞捕获在一根锥形光纤探针尖端、构成一个生物兼容的微观放大镜,实现了对细胞内结构的非标记成像和三维操控。相关成果于2019年7月3日发表在光学领域著名学术期刊 Light: Science & Applications(文章链接)。Light 期刊“最新研究进展”栏目以“Subwavelength imaging: Seeing smaller through cells”为题对该成果进行了报道。
为了从亚细胞层面甚至单分子水平去了解生命现象的本质,科学家一直在寻找能够探索微观世界的“眼睛”和“双手”。如斩获2014年诺贝尔化学奖的超分辨荧光显微镜为人们点亮了观察纳米物体的眼睛,而获得2018年诺贝尔物理学奖的光镊技术则提供了操控微小粒子的双手。然而,现有的光镊技术和超分辨成像技术独立于两个分离的光学系统,导致“眼睛”和“双手”无法相互配合。此外,由于这两种技术依赖高数值孔径物镜和细胞荧光标记,使其生物不兼容。如何将纳米“眼睛”和“双手”集成在一个生物兼容的器件中,是该领域急需解决的关键科学问题。针对这一问题,李宇超副教授等提出了一种新的近场成像和操控技术,将一个体内自然存在的酵母细胞、造血干细胞或红细胞捕获在一根光纤探针的尖端,以光纤作为手柄、细胞作为透镜构成了一个微观放大镜,光通过微观放大镜后汇聚成一个亚波长的光束,这个光束既能产生一个稳定的纳米光学势阱,又能充当一个近场的纳米照明光源,从而实现了对细胞内结构(如线粒体、小囊泡和细胞骨架)的光学成像和操控,成像分辨率和操控精度可达一百纳米。
该研究成果不但将“纳米手”和“纳米眼”融合在细胞研究中,而且不需要对细胞进行荧光标记,有望在生物传感和医学成像等研究中发挥作用。
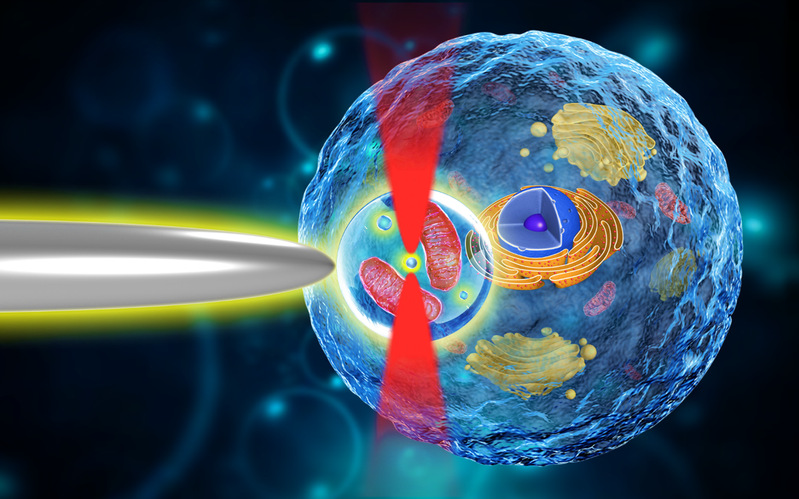
光纤探针和生物透镜构成的微观放大镜对细胞内结构进行成像和操控示意图